lunes, 14 de diciembre de 2015
domingo, 22 de noviembre de 2015
NORMAS PARA LA UTILIZACIÓN DE PRODUCTOS
QUÍMICOS
-
Evitar el contacto de los productos químicos con la piel. No pipetear con la boca, utilizad embudos para trasvasar líquidos y propipetas.
-
Si accidentalmente se vierte un ácido u otro producto químico corrosivo se debe consultar al profesor(ora).
-
Para detectar el olor de una sustancia, no se debe colocar la cara directamente sobre el recipiente: utilizando la mano abierta como pantalla, es posible hacer llega una pequeña cantidad de vapor hasta la nariz. Los frascos deben cerrarse inmediatamente después de su uso.
-
En la preparación de disoluciones debe agitarse de modo suave y controlado para evitar salpicaduras.
-
Los ácidos requieren un cuidado especial. Manipularlos con precaución y en la vitrina. Cuando queramos diluirlos, nunca echaremos agua sobre ellos; siempre al contrario es decir, ácido sobre agua.
 Vitrina de gases
Vitrina de gases
|
NORMAS DEL LABORATORIO
NORMAS DE SEGURIDAD EN EL
LABORATORIO
Normas generales
-
No fumes, comas o bebas en el laboratorio.
-
Utiliza una bata y tenla siempre bien abrochada, así protegerás tu ropa.
-
Guarda tus prendas de abrigo y los objetos personales en un armario o taquilla y no los dejes nunca sobre la mesa de trabajo.
-
No lleves bufandas, pañuelos largos ni prendas u objetos que dificulten tu movilidad.
-
Procura no andar de un lado para otro sin motivo y, sobre todo, no corras dentro del laboratorio.
-
Si tienes el cabello largo, recógetelo.
-
Dispón sobre la mesa sólo los libros y cuadernos que sean necesarios.
-
Ten siempre tus manos limpias y secas. Si tienes alguna herida, tápala.
-
No pruebes ni ingieras los productos.
-
En caso de producirse un accidente, quemadura o lesión, comunícalo inmediatamente al profesor.
-
Recuerda dónde está situado el botiquín.
-
Mantén el área de trabajo limpia y ordenada.
Normas para manipular
instrumentos y productos
-
Antes de manipular un aparato o montaje eléctrico, desconéctalo de la red eléctrica.
-
No pongas en funcionamiento un circuito eléctrico sin que el profesor haya revisado la instalación.
-
No utilices ninguna herramienta o máquina sin conocer su uso, funcionamiento y normas de seguridad específicas.
-
Maneja con especial cuidado el material frágil, por ejemplo, el vidrio.
-
Informa al profesor del material roto o averiado.
-
Fíjate en los signos de peligrosidad que aparecen en los frascos de los productos químicos.
-
Lávate las manos con jabón después de tocar cualquier producto químico.
-
Al acabar la práctica, limpia y ordena el material utilizado.
-
Si te salpicas accidentalmente, lava la zona afectada con agua abundante. Si salpicas la mesa, límpiala con agua y sécala después con un paño.
-
Evita el contacto con fuentes de calor. No manipules cerca de ellas sustancias inflamables. Para sujetar el instrumental de vidrio y retirarlo del fuego, utiliza pinzas de madera. Cuando calientes los tubos de ensayo con la ayuda de dichas pinzas, procura darles cierta inclinación. Nunca mires directamente al interior del tubo por su abertura ni dirijas esta hacia algún compañero. (ver imagen)
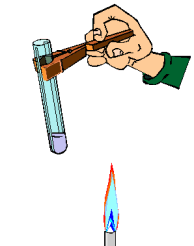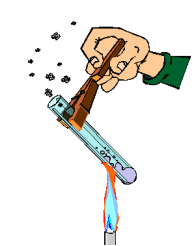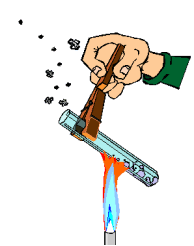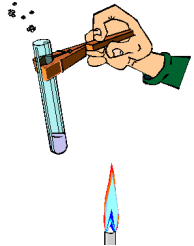
-
Todos los productos inflamables deben almacenarse en un lugar adecuado y separados de los ácidos, las bases y los reactivos oxidantes.
-
Los ácidos y las bases fuertes han de manejarse con mucha precaución, ya que la mayoría son corrosivos y, si caen sobre la piel o la ropa, pueden producir heridas y quemaduras importantes.
-
Si tienes que mezclar algún ácido (por ejemplo, ácido sulfúrico) con agua, añade el ácido sobre el agua, nunca al contrario, pues el ácido «saltaría» y podría provocarte quemaduras en la cara y los ojos.
-
No dejes destapados los frascos ni aspires su contenido. Muchas sustancias líquidas (alcohol, éter, cloroformo, amoníaco...) emiten vapores tóxicos.
sábado, 7 de noviembre de 2015
Método científico:Huevo que bota
HUEVO
EN VINAGRE
Este
experimento casero lo utilizaremos como ejemplo de las fases del
método científico (observación, planteamiento del problema,
hipótesis, experimentación, análisis y conclusiones).
Para
identificar estos fenómenos utilizaremos el método científico, que
consiste en la realización de una serie de procesos específicos que
utiliza la ciencia para adquirir conocimientos. Estos procesos
específicos son una serie de reglas o pasos bien definidos, que
permiten que al final de su realización se obtengan unos resultados
fiables y que aporten una explicación del porque del fenómeno
estudiado.
Se
podría definir un huevo como la célula de mayor tamaño que existe,
o como, un alimento muy completo y bastante frecuente en nuestra
gastronomía. Sin embargo, desde un punto de vista educativo es algo
mucho más amplio y complejo.
Se
pretende:
Al
poner un huevo en un recipiente conteniendo vinagre, observamos
ciertos cambios en sus propiedades físicas. Mediante esta
experimento casero nos abocaremos a detallar y explicar con mas
precisión cada uno de estos cambios físicos (color, olor, textura,
etc), así como también los posibles cambios en su estructura
química (descomposición).
Un
huevo de gallina consta de dos partes:
- La clara.
- La yema (parte nutritiva). Además su cáscara está formada por carbonato de calcio en un 94%.
- Huevos crudos de gallina.
¿QUÉ
NECESITAMOS?
* Vinagre.
*
bote de cristal.
*
Huevo.
¿Que debemos de hacer?
Se
toma un huevo de gallina y se sumerge en un bote que contiene
vinagre. Se tapa dicho frasco para evitar que el olor poco agradable,
tanto del ácido acético que forma el vinagre como del acetato de
calcio formado, salga al exterior.
Propósitos del
experimento:
Elaborar
el experimento de un huevo en vinagre a la perfección y que por
medio de esta actividad las personas puedan comprender la
importancia, que es conocer los cambios químicos que tienen los
cuerpos y las sustancias.
Explicación del
experimento.
El
huevo tras haberlo metido en vinagre en el vinagre (ácido
acético), produce una reacción química con dicho ácido y la
cáscara ( carbonato de calcio), originándose nuevas sustancias
- Una sal (que es en lo que se convierte la primera capa oscura de la cáscara al desprenderse)
- Un gas (por el cuál se aprecian las burbujas en las superficie del huevo)

Explicación
de preguntas individuales.
¿Por
qué el huevo pierde la cáscara?
La
cáscara del huevo se compone básicamente de carbonato cálcico
(CaCO3), que reacciona con los ácidos mediante la
siguiente reacción química:
CaCO3
+ 2 H+ -> Ca+2 + CO2 + H2O
En
esta reacción se forma dióxido de carbono, CO2, que se
desprende en forma de gas formando las burbujas que aparecen sobre la
cáscara del huevo, mientras que el agua y los iones calcio formados
se quedan disueltos en el vinagre, por lo que la cáscara queda
literalmente "destruida".
¿Por
qué se hincha?
Cuando
tenemos dos medios líquidos (con diferente concentración de sales)
separados por una membrana semipermeable, el agua es capaz de
atravesar dicha membrana desde el lado con menos sales al más
salino, para intentar igualar la concentración a ambos lados.
Existe
la creencia de que "la sal engorda". En realidad, si
tomamos mucha sal, la concentración de ésta en nuestras células
aumenta, por lo que el agua entrará en ellas para intentar rebajar
dicha concentración, dando como resultado que las células se
hinchen. Este efecto se suele conocer como "retención de
líquidos".
Volvamos
al huevo: por debajo de la cáscara existe una especie de "tela"
que separa la clara de la cáscara. Esta "tela" es una
membrana semipermeable, que deja pasar agua del vinagre (en el que la
concentración de sales es menor) al huevo. Como consecuencia de la
entrada de agua en el huevo, éste aumenta su volumen.
¿Y
por qué se queda como una goma?
Cuando
freímos un huevo, las proteínas de la clara se ven sometidas a una
temperatura muy alta, lo que provoca su transformación en una
proteína en estado sólido cuya estructura interna es diferente a la
inicial. Este proceso es, además, irreversible, y recibe el nombre
de desnaturalización.
El
proceso de desnaturalización ocurre cuando la proteína es sometida
a cambios de temperatura (por ejemplo, cuando freímos el huevo) o a
cambios de pH (por ejemplo, cuando la ponemos en contacto con un
ácido o una base).
En
nuestro caso, cuando el agua atraviesa la membrana semipermeable que
encierra la clara del huevo, lo hace acompañada de ácido acético
(responsable de la acidez del vinagre), por lo que al mismo tiempo
que el huevo se hincha comienza la desnaturalización de la albúmina
de la clara. La proteína desnaturalizada formará una capa gruesa
que dará el aspecto de pelota al huevo.
Sin
embargo, esta capa también llegará a impedir que siga entrando agua
con ácido acético a la parte más interna del huevo, por lo que por
dentro el huevo quedará crudo, así que cuidado: si lo dejamos caer
con demasiada fuerza, el huevo reventará y nuestro experimento se
irá al garete
martes, 20 de octubre de 2015
Presentación del blog
Me llamo Mario y soy de la clase de 4ºC.La profesora de ¨Técnicas del laboratorio¨ nos ha pedido que hagamos un blog de todo lo que hagamos en cada clase ( o algo de eso ha dicho,no me he enterado muy bien de lo que dijo). Se supone que tengo que hacer algo de notación científica de un experimento pero como el otro día (12/10/2015) parece ser que dijo que teníamos que traer los materiales necesarios para hacer un experimento en clase,en el cual tendríamos que decir en que se basa el experimento o algo de eso...que tendríamos que hablar de él en definitiva.Pero como yo soy un máquina y no escuché nada pues no lo he hecho y solo hago esta introducción en el último día de entrega...
FIN
 |
| Cuéntamelo como bueno Mila 0_o |
Suscribirse a:
Entradas (Atom)